最近の研究(1)
生体内におけるDNA分解の必要性 ー DNase IIノックアウトマウスの解析から
DNase IIは酸性DNA分解酵素のひとつで、マクロファージを含むほぼ全ての細胞に発現している。細胞内においてDNase IIはリソソームに局在しており、マクロファージが貪食したアポトーシス細胞の染色体DNAの分解を担っている。
1) DNase IIノックアウトマウスの作成
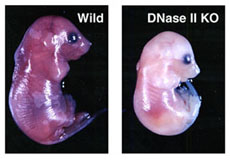
(左)Wild(野生型)にくらべ(右)KO(ノックアウト)は
体全体が白くなってるのがわかる
DNase IIノックアウトマウスの胎仔は胎生致死であり、赤血球の数が正常マウスの十分の一以下という重篤な貧血症を呈していた 。胎仔の肝臓には異常な病巣が多数観察され、電子顕微鏡による観察から、この病巣が未分解DNAを含む多数の核を抱え込んだマクロファージからなることがわかった。
胎生期において肝臓は造血を担う場であり、未分化な赤芽球が赤血球を分化する際に大量の核が産生される(脱核)。電子顕微鏡像より、赤血球から放出された核はマクロファージによって貪食されており、貪食された核に含まれる染色体DNAはマクロファージ内のDNase IIにより分解されていることがわかった。
それでは、何故DNase IIのノックアウトマウスは貧血を呈すのだろうか?
2) DNase IIノックアウトマウスの貧血は、未分解のDNAを蓄積したマクロファージが産生する IFN-β(インターフェロンβ)が原因である
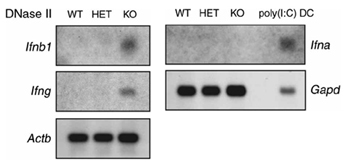
代表的なIFN誘導遺伝子のノザンブロット
野生型およびDNase IIノックアウトマウスの胎仔肝臓からRNAを調製しGene arrayによって解析したところ、DNaseII ノックアウトマウスでは、IFNによって発現誘導される遺伝子が多数活性化していることがわかった。
WT(野生型),HET(ヘテロ), KO(ノックアウト))。また、in situ ハイブリダイゼーション法により、未分解の核を蓄積した胎仔肝臓マクロファージはtype I IFNのひとつであるIFNβを発現していることが明らかとなった。
DNaseII とtype I IFN受容体のダブルノックアウトマウスでは貧血が回復したことから、未分解DNAを蓄積したマクロファージによって産生されるIFN-βが致死的な貧血の原因となっていることが示された。
現在、何故IFN-βが致死性貧血の原因となるのか解析しています。
3) 生体内おけるDNA 分解異常が引き起こす疾患ー慢性多発性関節炎
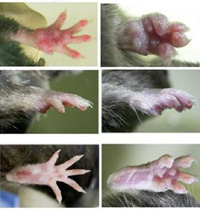
(左)野生型、(右)DNase II決失マウス。
決失マウスでは足の関節が腫れている
胎仔のDNase IIの役割について解析してきたが、生体内(=生後マウス)におけるDNase IIの役割は何だろうか?生体内でDNA分解がなされないと、どのようなことが起こるのだろうか?
DNase II遺伝子の生体内における作用を調べるため、 [poly(IC)]という物質を投与することでDNase II遺伝子を決失するマウスを作成した。このマウスは胎生期ではpoly(IC)を投与していないのでDNase IIは正常に働くが、生後任意の時期ににpoly(IC)を投与するとDNase II遺伝子が決失しマクロファージ内でのDNA分解ができなくなる。
私たちは、このマウスがヒトの関節リウマチと似た関節炎を発症することを見出した。DNAが残存しているマクロファージは活性化してTNFを産生しており、発症した関節ではTNF、IL-6やIL-1bなどのサイトカイン遺伝子の発現が大きく増加していた。さらに、血清中にはリウマチ因子などが高濃度に認められた。このマウスに、まだ関節炎を発症していない時期に抗TNF抗体を投与すると、関節炎の発症を抑制することができ、関節炎を発症したマウスに抗TNF抗体を投与すると関節の腫れは減少し、サイトカイン遺伝子の発現も顕著に減少した。これらの結果より、マクロファージの異常な活性化が関節リウマチの原因のひとつであることがわかった。さらに、生体内では赤血球分化の際に放出される核やアポトーシス細胞を処理するために毎日膨大な量のDNAを分解しているが、これらのDNA分解が効率よく起こらなければ関節炎を発症する可能性があることを示している。
さらに詳しくは http://www.fbs.osaka-u.ac.jp/publications/nagata2006-1/
4) 赤血球分化の際に放出される核のホスファチジルセリン依存的な貪食機構
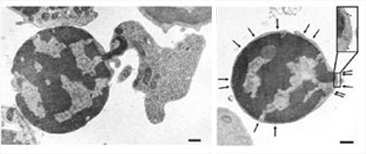
(写真左)右の不定形な細胞が核を放出しかけている網状赤血球で
左が放出されようとしている核。
中央のくびれている部分でかろうじて繋がっている。
この状態ではマクロファージに認識されない
(写真右)網状赤血球から完全に切り離された放出核。
矢印の示している場所がホスファチジルセリン陽性の箇所。
ところで、放出された核はどのような機構でマクロファージに取り込まれるのだろうか?ヒトの身体では毎日、2 x 1011個の赤血球が産生されるが、この細胞には核はない。ということは2 x 1011個もの核が毎日放出され、マクロファージによって貪食処理されていることになる。この大量の放出核をマクロファージはどのような機構で認識し、貪食しているのだろうか?
私たちはマクロファージと核を放出する直前の網状赤血球を共培養することにより、マクロファージによって核が貪食されるのは核と網状赤血球の結合が切断された後に起こることを見い出した。すなわち、網状赤血球から切り離されると核はホスファチジルセリンを細胞表面上に露出することを明らかにした。ホスファチジルセリンは、アポトーシス細胞がeat meシグナルとして用いている脂質で、死細胞でのみ細胞膜上に露出されることが知られている。マクロファージ上に存在するホスファチジルセリン受容体によって認識され、死細胞の効率的な貪食に貢献している。
これらのことから、赤血球から放出された核も、アポトーシス細胞と同様の機構で認識・貪食されることが明らかとなった。
